Progettazione e sintesi di oligonucleotidi per uso diagnostico e terapeutico
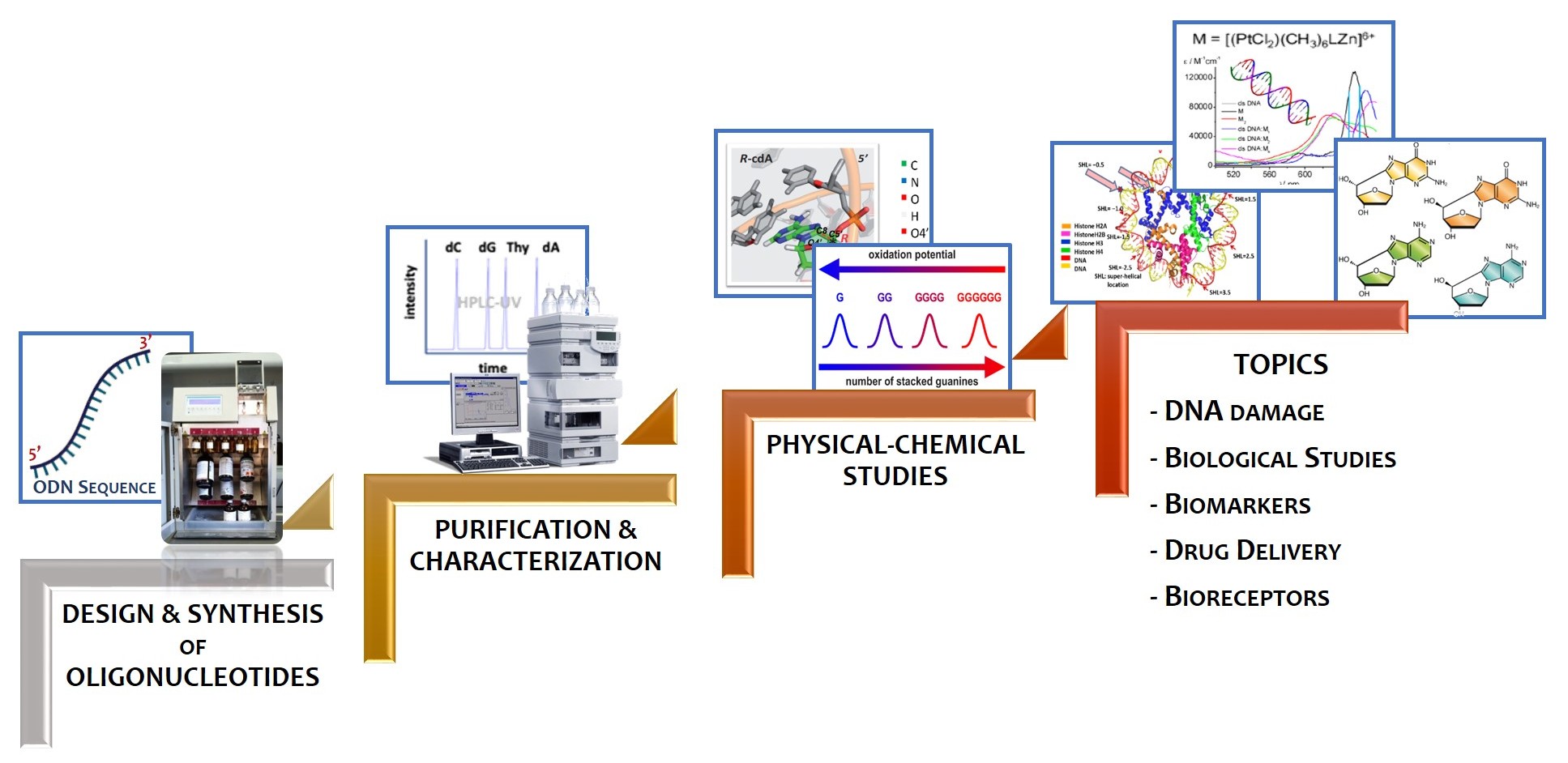
L’attività di ricerca è prevalentemente rivolta alla progettazione e sintesi di derivati di acidi nucleici, sia per la realizzazione di modelli biomimetici oligonucleotidici, per studi in vivo ed in vitro, sia per la sintesi di nuovi farmaci antivirali analoghi nucleosidici.
Gli oligonucleotidi (ODNs) trovano impiego in una vasta gamma di applicazioni dalle ricerche biologiche, biomediche e nanotecnologiche fino all’ambito terapeutico e diagnostico. Mediante la sintesi automatica utilizzando il metodo delle fosforamiditi, commerciali o opportunamente sintetizzate, abbiamo sviluppato nuovi derivati oligonucleotidici con caratteristiche specifiche in funzione della ricerca di interesse.
Sequenze ODNs, modificate e non, rappresentano i modelli biomimetici per gli studi sul danno ossidativo al DNA, sistema di riparazione enzimatico e individuazione di lesioni puriniche (8-oxo-purine e 5’,8-cyclopurine). Grazie ad un sofisticato protocollo analitico tali lesioni sono state individuate nel DNA genomico e mitocondriale di modelli cellulari neurodegenerativi; in biopsie di tessuto di pazienti affetti da Morbo di Crohn, Colite Ulcerosa e fortemente obesi evidenziano l’associazione tra stress ossidativo e malattie infiammatorie. Tale approccio multidisciplinare ha lo scopo di individuare potenziali nuovi biomarcatori associati a tali patologie.
Oggetto di ricerca è anche lo studio dell’interazione di modelli ODNs (G-quadruplex, TFOs, etc.) con molecole farmacologicamente attive, proteine e ioni metallici, che trovano applicazione sia come agenti terapeutici, che nella realizzazione di sonde chirali biocompatibili (es. Carbon based nanoparticles/ODNs).
E’ inoltre argomento di studio lo sviluppo di nuovi farmaci ad azione antivirale analoghi di nucleosidi.
– Increased Levels of 5′,8-Cyclopurine DNA Lesions in Inflammatory Bowel Diseases. Masi, A.; Fortini, P.; Krokidis, M.G.; Romeo, E.F.; Bascietto, C.; De Angelis, P.; Guglielmi, V.; Chatgilialoglu, C. Redox Biol. 2020, 34, 101562.
– Oxygen Dependent Purine Lesions in Double-Stranded Oligodeoxynucleotides: Kinetic and Computational Studies Highlight the Mechanism for 5′,8-Cyclopurine Formation. Chatgilialoglu, C.; Eriksson, L.A.; Krokidis, M.G.; Masi, A.; Wang, S; Zhang, R. J. Am. Chem. Soc. 2020, 142, 5825–5833.
– Diastereomeric Recognition of 5′,8-cyclo-2′-Deoxyadenosine Lesions by Human Poly(ADP-ribose) Polymerase 1 in a Biomimetic Model. Masi, A.; Sabbia, A.; Ferreri, C.; Manoli, F.; Lai, Y.; Laverde, E.; Liu, Y.; Krokidis, M.G.; Chatgilialoglu, C.; Faraone Mennella, M.R. Cells 2019, 8, 116.
– Pyrazinoporphyrazines with Externally Appended Pyridine Rings. 13. Structure, UV-Visible Spectral Features, and Noncovalent Interaction with DNA of a Positively Charged Binuclear (Zn-II/Pt-II) Macrocycle with Multimodal Anticancer Potentialities. I. Manet, F. Manoli, M.P. Donzello, E. Viola, A. Masi, G. Andreano, G. Ricciardi, A. Rosa, L. Cellai, C. Ercolani, and S. Monti. Inorganic Chemistry 2013, 52, 321-328.


